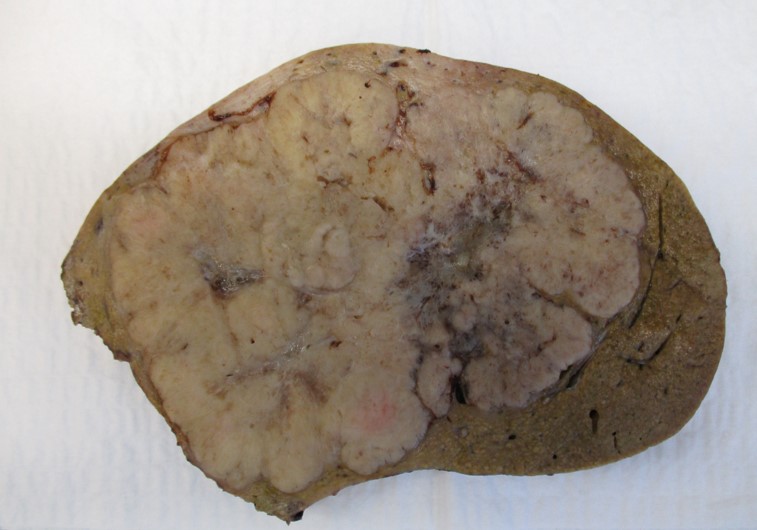
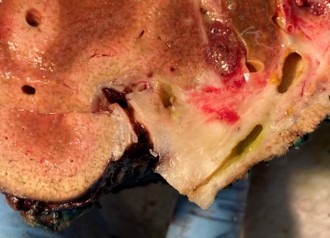
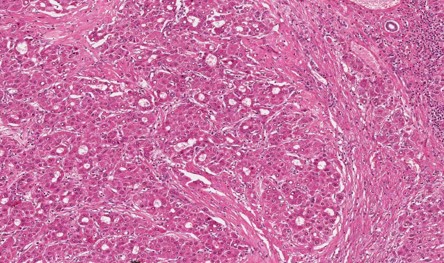
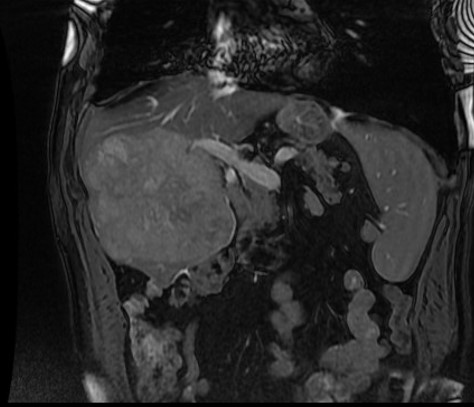
Metastasi epatiche da neoplasia colorettale
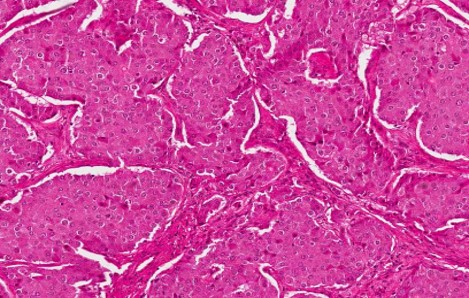
Il fegato è frequente sede di metastasi da tumori primitivi dell’apparato digerente, ma può in realtà essere interessato da localizzazioni di qualsiasi tipo di tumore, a causa della notevole quantità di sangue che lo attraversa e della funzione di filtro che esso svolge.
L’ asportazione chirurgica di tumori secondari del fegato (metastasi) può essere opportuna per migliorare la sopravvivenza a lungo termine nei casi di metastasi da tumore primitivo del colon-retto o da tumori neuroendocrini. Nei restanti tumori secondari, in genere la resezione epatica non risulta modificare significativamente la sopravvivenza del paziente e dunque non appare di principio indicata, pur con alcune eccezioni valutabili caso per caso (es. tumore del rene, della mammella, dell’ovaio, dello stomaco, melanoma), mentre sono necessari programmi di trattamento farmacologico (chemioterapia) differenti in rapporto alla natura e alla sede del tumore primitivo.
Il fegato rappresenta la sede più frequente di metastasi da carcinoma colorettale e, nella maggioranza dei casi, l’interessamento epatico determina la durata e la qualità di vita del paziente.
Circa il 50% dei pazienti con tumore colo-rettale sviluppa o svilupperà metastasi epatiche durante il corso della malattia (15-25% dei pazienti presenta metastasi epatiche alla diagnosi, mentre nei restanti casi le metastasi epatiche insorgono in periodi diversi dell’evoluzione clinica della malattia): si tratta quindi di un problema molto diffuso.
I notevoli progressi nelle tecniche chirurgiche e farmacologiche e nella conoscenza della malattia hanno reso il tumore metastatico del fegato sempre più curabile, tanto che circa un paziente su tre con metastasi epatiche da tumore del colon-retto può sottoporsi a trattamenti con l’obiettivo di curare la malattia che con molta probabilità non si ripresenterà nei dieci anni successivi.
La resezione chirurgica costituisce attualmente il trattamento di prima scelta per i pazienti portatori di metastasi da carcinoma colo-rettale. Nessuna modalità alternativa di trattamento, sia locale (termoablazione mediante radiofrequenza, alcolizzazione) sia generale (chemioterapia) ha sino ad ora dato risultati simili alla chirurgia. In effetti, la sopravvivenza a 5 anni dall’intervento dei pazienti sottoposti a resezione epatica per metastasi da carcinoma colorettale è compresa tra il 16% ed il 49%, percentuali che rappresentano risultati incoraggianti rispetto alla sopravvivenza dei pazienti non trattati (0-3%). La resezione chirurgica consente inoltre significative sopravvivenze e lungo termine (17%-33% a 10 anni). Va infine segnalato che, sebbene la percentuale di ripresa delle metastasi epatiche dopo l’intervento di resezione sia significativa (40%), un ulteriore intervento di asportazione ha comunque un beneficio significativo sulla sopravvivenza (30% a 5 anni) e, dunque, deve essere preso in considerazione.
Le possibilità di successo della chirurgia resettiva per metastasi da carcinoma colorettale variano in funzione di vari elementi, alcuni dei quali legati al tumore primitivo (aggressività biologica, stato di avanzamento del tumore al momento della diagnosi), altri legati alle metastasi stesse (numero, dimensioni, distribuzione nel fegato).
I diversi fattori che influenzano la sopravvivenza del paziente dopo asportazione chirurgica di metastasi da carcinoma colorettale possono essere combinati per creare dei punteggi di rischio (“risk score”) per recidiva della malattia a distanza. I più noti sono lo score del Memorial Sloan-Kettering Cancer Center di New York (score di Fong), lo score francese (score di Nordlinger) e lo score giapponese (score di Makuuchi).
E’ sempre bene ricordare che la diagnosi e il trattamento del paziente con metastasi epatiche da tumore colorettale necessita un approccio multidisciplinare con l’intervento sinergico di chirurghi, radiologi, oncologi e radioterapisti: le scelte terapeutiche (chirurgia, chemioterapia ecc.) devono essere condivise dai diversi specialisti del team e dal paziente, per ottimizzare il percorso di cura e ottenere buoni risultati a breve e lungo termine.

In molti casi le metastasi epatiche restano asintomatiche per molto tempo e non possono essere individuate con la semplice palpazione fino a che non hanno raggiunto dimensioni notevoli.
Con il passare del tempo, però, la presenza di metastasi può compromettere le funzioni del fegato e dare sintomi come febbricola, sensazione di pesantezza nella parte alta dell’addome, dolore al fianco destro, stanchezza, perdita di peso e di appetito, nausea, ittero, confusione mentale. Attualmente non esistono strategie di prevenzione efficaci (oltre alla chemioterapia) per impedire a un tumore di dare metastasi al fegato.
La migliore prevenzione resta, quindi, l’identificazione precoce del cancro primario e l’esecuzione regolare dei controlli per individuare per tempo eventuali recidive. Inoltre, dal momento che le metastasi epatiche si possono sviluppare mesi o anni dopo la diagnosi del tumore primario, i controlli al fegato sono comuni per molti tipi di tumore (primo tra tutti quello del colon-retto) anche dopo la sospensione delle terapie.
Nel caso di segni e sintomi che possono far pensare alla presenza di metastasi al fegato (precedente tumore con tendenza a dare metastasi epatiche, perdita di peso e di appetito, nausea, dolore addominale, ittero), il medico prescrive esami del sangue per valutare il funzionamento del fegato e il livello di alcuni marcatori tumorali come CEA e CA-19.9, che risultano elevati, per esempio, nel caso di metastasi da tumore del colon-retto anche dopo che il tumore primario è stato asportato.
Per caratterizzare meglio le eventuali metastasi al fegato sono però necessari esami di diagnostica per immagini: ecografia, risonanza magnetica, tomografia computerizzata (TC), tomografia a emissione di positroni (PET) permettono di capire con esattezza quante sono le metastasi, quanto sono estese e dove si trovano.
La biopsia, cioè il prelievo di tessuto epatico da analizzare poi al microscopio, è effettuata solo nei casi che restano dubbi dopo gli esami elencati.
Come detto in precedenza, la chirurgia rappresenta il trattamento di scelta e l’unico con intento curativo (trattamento gold standard).
La possibilità di intervenire chirurgicamente dipende essenzialmente dalla coesistenza di due condizioni: asportazione completa della malattia e preservazione di una quantità di fegato sufficiente per il sostegno delle funzioni vitali nel periodo postoperatorio. Ricordiamo infatti che il fegato ha la capacità di rigenerare se stesso ritornando alle dimensioni ed alle funzioni iniziali dopo un intervento chirurgico, ma che questo processo richiede alcuni mesi.
Il rischio di insufficiente funzione del fegato dopo resezione chirurgica è considerato basso se viene mantenuto almeno il 40% del fegato, moderato per quantità residue di fegato comprese tra 40% e 25%, elevato per quantità inferiori al 25%. Nei casi nei quali le due condizioni suddette non coesistono, l’asportazione chirurgica può essere riconsiderata mettendo in atto strategie specifiche per ridurre il volume delle metastasi prima dell’intervento (chemioterapia neoadiuvante) o incrementare la quantità di fegato da preservare (portoembolizzazione preoperatoria). È anche possibile programmare di asportare tutte le metastasi attraverso due interventi a distanza di 1-2 mesi (“two-stage hepatectomy”), per consentire al fegato di rigenerare tra un intervento ed il successivo o a distanza più ravvicinata attraverso una nuova procedura, riservata a casi molto selezionati, chiamata ALPPS (Associating Liver Partitioning and Portal vein ligation for Staged hepatectomy).
In generale, l’intervento chirurgico consiste nella asportazione della lesione tumorale e di una porzione circostante di fegato, affinché vi sia almeno 1 cm di tessuto sano tra il margine del tumore e la linea di sezione del fegato, sebbene in condizioni particolari sia accettabile anche un margine di tessuto sano meno spesso, se ciò può consentire l’asportazione completa del tumore preservando quantità sufficienti di fegato.
Nei pazienti con metastasi epatiche sincrone al tumore colorettale (quando cioè le metastasi vengono diagnosticate contemporaneamente al tumore primitivo, durante gli esami di stadiazione), i noduli possono essere asportati nel corso dell’intervento di rimozione del tumore al colon: il paziente viene quindi trattato con un solo intervento chirurgico e durante un’unica ospedalizzazione. Inoltre in casi selezionati di metastasi sincrone in cui non è possibile intervenire direttamente sui due fronti e dove l’estensione della malattia epatica condizionerebbe significativamente la prognosi del paziente, si può procedere all’asportazione delle metastasi epatiche prima della rimozione del tumore primitivo (approccio liver first).
Sebbene tradizionalmente l’indicazione alla asportazione chirurgica sia riservata solo ai pazienti con metastasi esclusivamente nel fegato, recenti studi suggeriscono incoraggianti risultati a distanza anche nei portatori di metastasi nel fegato ed in sedi addominali extraepatiche (linfonodi, peritoneo, surreni) o extraaddominali (polmone), purché l’intervento porti alla asportazione di tutte le aree tumorali.
La percentuale di pazienti suscettibili di trattamento chirurgico al momento della diagnosi è tuttavia non superiore al 20-30% dei casi; il numero di metastasi e/o la loro posizione nel fegato (infiltrazione di grandi vasi sanguigni) e/o l’entità della sostituzione del fegato sano da parte del tumore precludono infatti spesso la possibilità della resezione chirurgica. In questi casi, la chemioterapia rappresenta la modalità di trattamento idonea.
Il recente sviluppo di agenti chemioterapici più efficaci, quali l’oxaliplatino e l’irinotecan, ha consentito di raggiungere importanti traguardi in ambito oncologico, infatti ha consentito di ottenere, in un crescente numero di pazienti, una riduzione significativa della massa tumorale e un incremento della sopravvivenza dei pazienti metastatici non operabili, oltre ad apparire in grado di aggiungere al gruppo di pazienti idonei a chirurgia un 10-20% di pazienti inizialmente non resecabili.
La chemioterapia sistemica viene spesso proposta ai pazienti con metastasi da tumore colorettale (anche ai candidati a chirurgia, con poche eccezioni), prima (chemioterapia neoadiuvante) e/o dopo (chemioterapia adiuvante) l’intervento al fegato, proprio in quanto permette di consolidare i risultati a lungo termine della chirurgia.
I farmaci vengono generalmente somministrati in vena (via endovenosa) per ottenerne la distribuzione in tutto l’organismo (chemioterapia sistemica). Nel caso di metastasi esclusivamente epatiche però, può essere anche considerata la possibilità di somministrazione direttamente nel fegato (chemioterapia locoregionale) attraverso un vaso sanguigno arterioso (chemioterapia intraarteriosa). Con questa metodica è possibile infatti infondere nel fegato farmaci che risultano molto efficaci sulle metastasi e che, pur altamente tossici per l’organismo, vengono somministrati a dosi molto elevate senza particolari effetti collaterali in quanto il farmaco viene distrutto da fegato stesso prima che possa raggiungere il resto dell’organismo.